eVooZ, l'eCRF de recherche clinique simple et abordable
Vous êtes promoteur d’un essai clinique et vous avez besoin d’un eCRF facile à utiliser, abordable, et infiniment plus fiable et conforme qu’un tableur ou un formulaire?

L'eCRF eVooZ, qu'est-ce que c'est ?
eVooZ est un cahier de données électroniques en ligne, hébergé sur un serveur certifié HDS,multilangues, facile à utiliser et disposant de toutes les fonctions nécessaires à votre projet de recherche clinique. Il a été pensé et optimisé par un ARC de terrain pour être rapide et agréable à l’usage.

Une interface simple
eVooZ est organisé avec des pages indépendantes et un menu horizontal. Vous pouvez voir la liste de vos patients, completer et éditer les données, enregistrer ou verrouiller vos données.

Un outil complet
eVooZ est multi-utilisateur, multi-centrique, multi-statut. Vous pouvez randomiser, monitorer vos données, et vous disposez d’un audit trail et de multiples autres fonctions.

Un prix abordable
eVooZ est abordable pour les petites structures hospitalières, sans pour autant négliger l’aide et le conseil. Nous vous aidons à la rédaction du CRF papier, puis nous créons pour vous la version électronique, prête à l’emploi !
Questionnaire en ligne
eVooZ est un cahier de données électroniques en ligne, sur un serveur sécurisé avec des comptes individuels ou par centre.
Les données sont éditables, verrouillables, imprimables ; elles sont enregistrées dans une base de données MySQL et exportable en CSV (Excel®). Le CRF est multilangue.
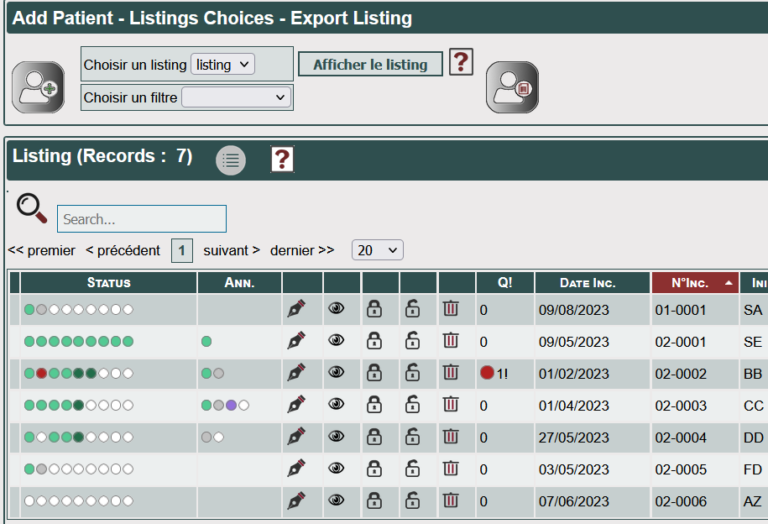
Monitorage à distance
Chaque donnée est monitorable localement ou à distance, avec un compte « monitor » dédié, sans accès en écriture.
Les valeurs peuvent également être définies comme ‘ND’, ‘NA’, ‘NF’. Des contrôles automatiques bloquants ou non bloquants sont également paramétrables.
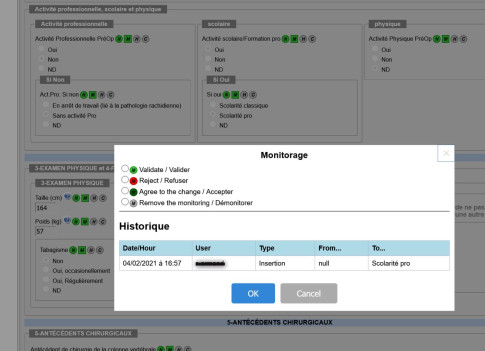
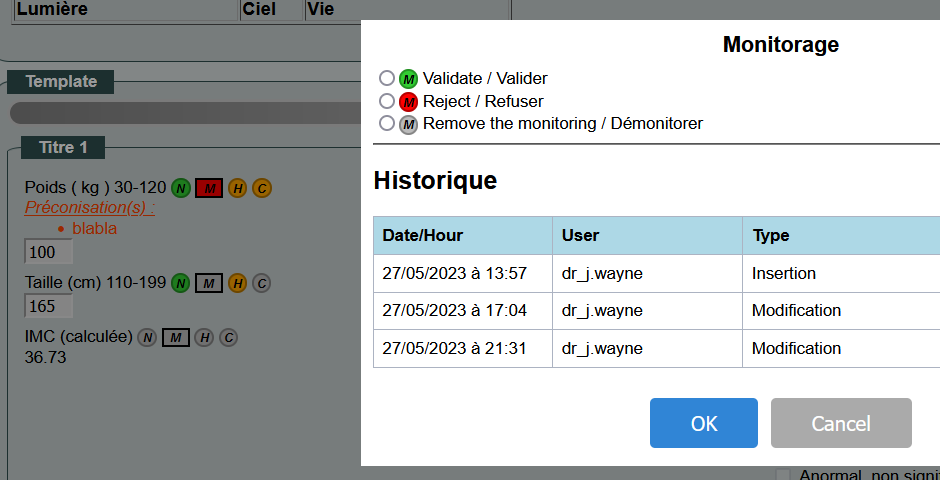
Historique des modifications
La fonction « historique » enregistre chaque modification des variables.
Vous pouvez ainsi retrouver chaque modification de donnée, avec la date et l’utilisateur.
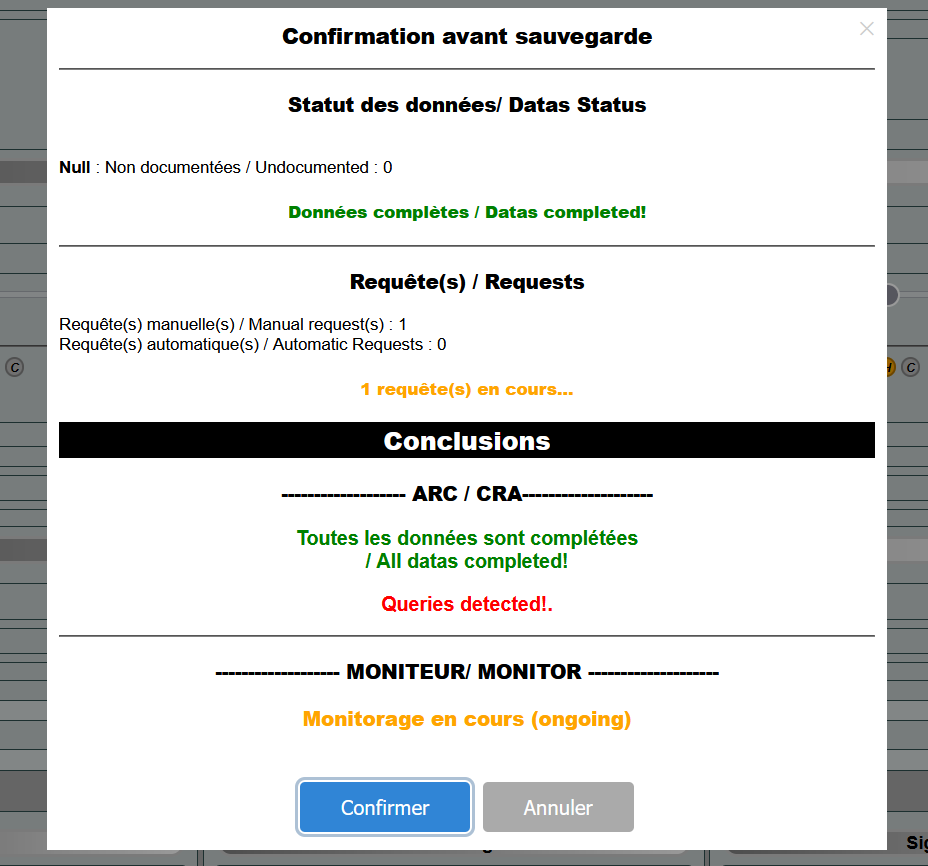
A chaque enregistrement de page, Evooz vérifie la complétion des données et informe l’utilisateur des éventuelles données manquantes sans pour autant le bloquer et modifie intelligemment le statut de la page.
Des messages clairs s’affichent pour aider l’utilisateur à chaque étape!
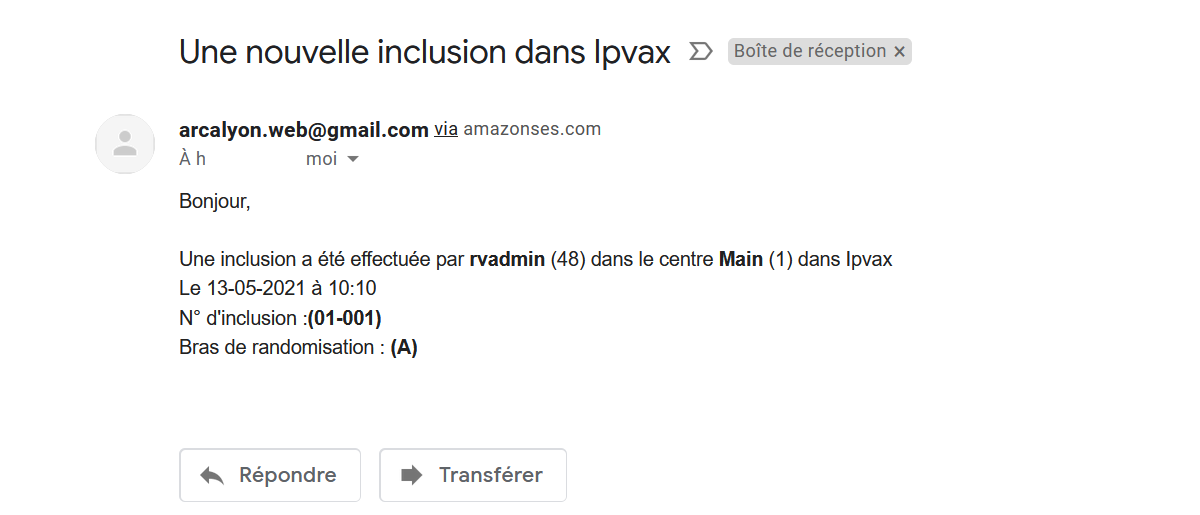
Inclusion par email
Envoi d’emails à l’inclusion, ou pour chaque EIG déclaré, à des destinataires prédéterminés ( Chefs de projet, Coordonateur de l’étude, Pharmacovigilance).
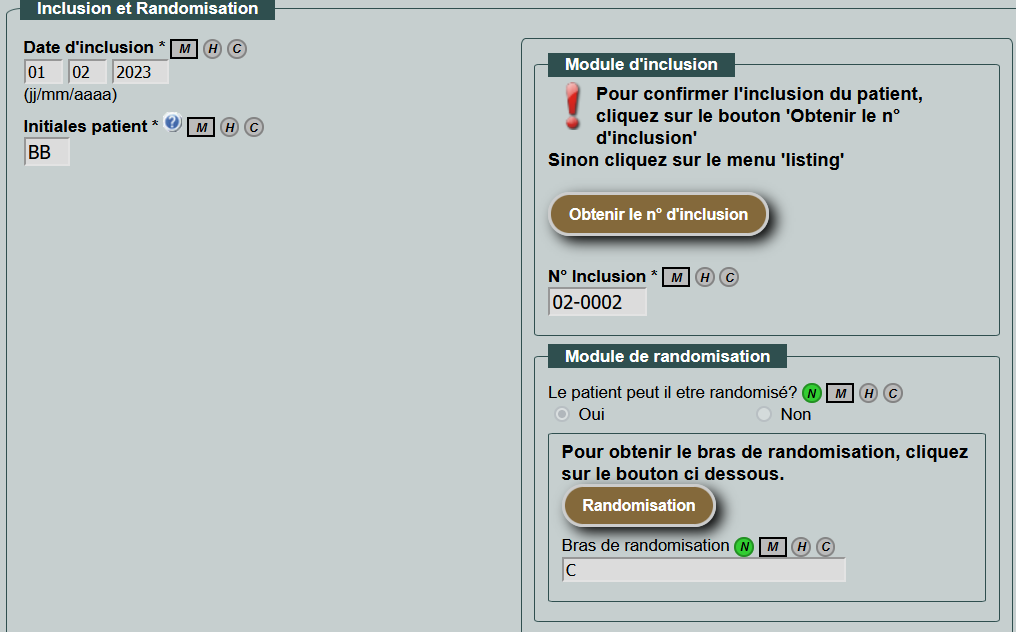
Possibilité de randomisation
eVooZ offre la possibilité de randomisation active ou passive, avec ou sans stratification.
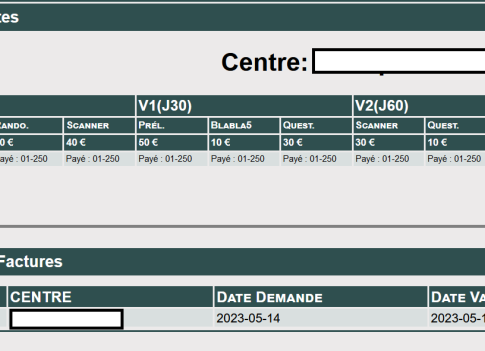
Gestion de la facturation
Evooz peut vous aider à gérer la facturation de vos centres: Les données de facturations sont éditées à la demande, après validation par l’ARC moniteur
L’Arc terrain et le moniteur savent à chaque instant ce qui a été payé et sur quelle facture.
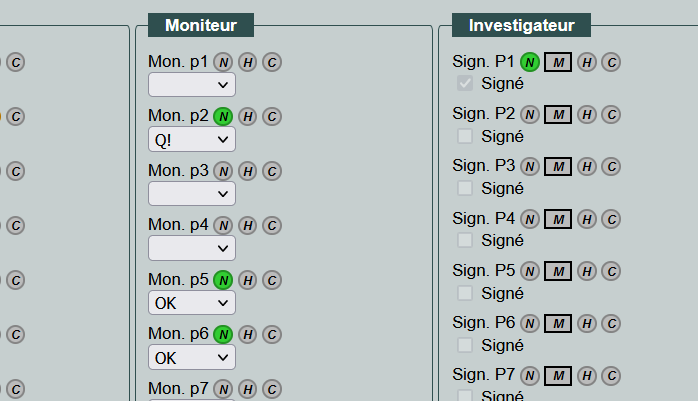
Signatures
Les comptes de type « Investigateur » peuvent également signer les pages de l’eCRF ou celui du patient en entier.
E-mailing
Il est possible d’envoyer des emails de rappels aux centres, à fréquence fixe ou en fonction des dates de visites prévues.

Interface personnalisable
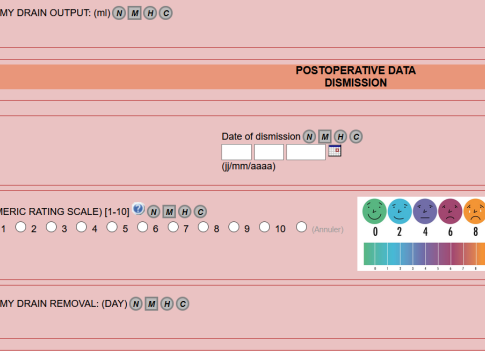
eVooZ permet d’agrémenter l’eCRF de popups « conseils », de liens externes, d’images, de schémas ou toutes autres aides qui pourraient améliorer la qualité des données.
Contrôles intelligents
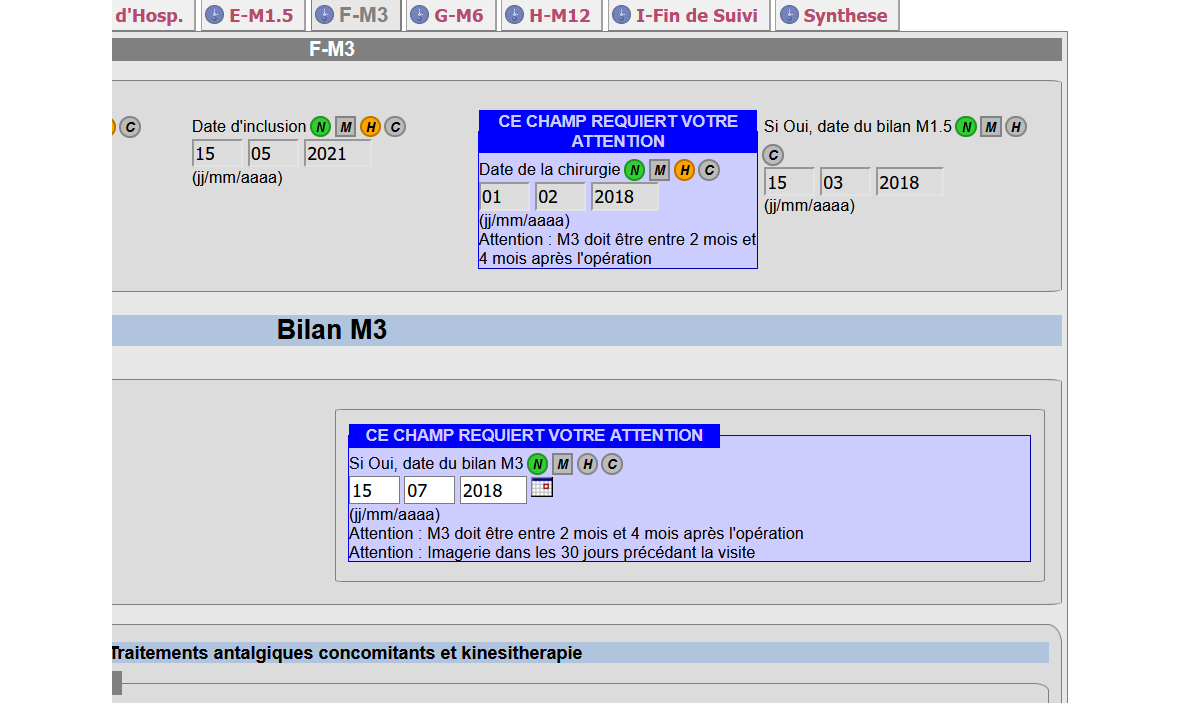
Contrôles automatiques et paramétrables des données : bloquants ou non bloquants, en language SQL (puissance illimitée).
Le controle peut s’effectuer sur une seule variable, mais également sur plusieurs variables liées.
Coût adapté au projet
Notre objectif est que chacun, centre hospitalier promoteur ou CRO, puisse accéder à un CRF professionnel.
Vous voulez en savoir plus sur l'eCRF eVooZ ?
N’hésitez pas à nous contacter pour planifier un rendez-vous pour une démonstration du logiciel.
Nous serons ravis de répondre à toutes vos questions.
Qu'est qu'un eCRF ?
L’eCRF est tout simplement une version électronique du CRF traditionnel. CRF est un acronyme couramment utilisé pour Case Report Form, un formulaire utilisé pour la saisie de données dans les essais cliniques de produits pharmaceutiques et de dispositifs médicaux.
Historiquement, les formulaires de rapport de cas (CRF) ont toujours été rédigés sur une sorte de papier carbone, afin qu’une feuille puisse être ajoutée au Trial Master File (TMF). Les CRF de style classique sont encore utilisés dans les petites études et ils ont encore leur place. Mais la plupart des études à plus grande échelle ont désormais adopté les eCRF.
Quels sont les avantages d'un eCRF vs un CRF ?
Nous savons que l’eCRF est le grand frère technologique du système CRF traditionnel. Alors, quels en sont les avantages ?
- Disponibilité des données – où que ce soit et à tout moment, vous pouvez avoir besoin de consulter les détails.
- Transfert rapide des données à partir de dispositifs externes
- Contrôles de plausibilité prédéfinis pour s’assurer que les données semblent appropriées
- Possibilité de partager les données, si d’autres personnes concernées ont besoin d’accéder aux informations.
- Rapports – rapports d’état disponibles tout au long de l’étude et à son terme.
- Sécurité – vous êtes le seul à déterminer et à contrôler la sécurité. Mais comme la sécurité est importante pour tout ce que nous faisons avec les données des essais cliniques, cette approche offre des systèmes de stockage et d’accès beaucoup plus sûrs que les CRF traditionnels.
Bien que les CRF traditionnels aient encore une certaine place dans l’environnement des essais cliniques, ils vont progressivement disparaître avec le développement de la technologie. Un long système de rapport sur papier ne peut certainement pas rivaliser longtemps avec quelques touches sur un téléphone ou une tablette…
L’eCRF est un formulaire de rapport de cas électronique qui remplace le CRF traditionnel. Ces systèmes sont conçus pour faire gagner du temps et contribuer à rendre les données plus transparentes pour toutes les personnes impliquées dans le processus d’essai clinique.